mRNA作為一種中間載體,能夠將DNA中的遺傳密碼傳遞到核糖體中進行蛋白質表達,在疫苗、蛋白質替代治療和基因編輯等方面具有巨大的潛力。與傳統的小分子和蛋白藥物相比,基于mRNA的療法在安全性、效力和制備方面都顯示出一些特定的優勢。
然而,盡管mRNA具有這些潛在的優勢,但如何安全高效且和穩定地進行細胞內遞送仍然是mRNA的一個重要障礙。近年來,納米生物技術取得了重大進展,為開發mRNA納米載體提供了重要的工具。納米載體系統可直接用于在生物微環境中裝載、保護和釋放mRNA,并可用于刺激mRNA翻譯以制定更有效的干預策略。因此,設計新一代的納米材料將可能引發了mRNA技術的革命。
脂質納米顆粒是臨床上最先進的mRNA載體。LNP為mRNA遞送提供了許多好處,包括制劑簡單、模塊化、生物相容性和較大的mRNA有效載荷容量。除RNA藥物外,LNP通常包括四種成分,可電離脂質、膽固醇、輔助磷脂和聚乙二醇化脂質,它們共同封裝和保護脆弱的mRNA。
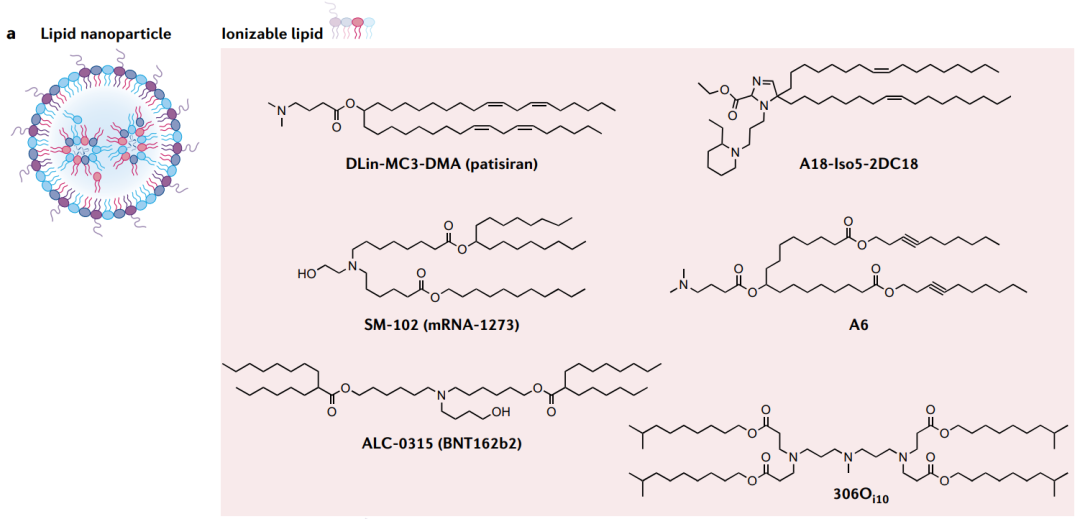
可電離脂質與mRNA在酸性緩沖液中形成納米顆粒,使脂質帶正電荷并吸引RNA。此外,它們在內涵體的酸性環境中帶正電荷,這促進了它們與內涵體膜的融合,將其釋放到細胞質中。
DODAP和DODMA是第一種用于RNA輸送的可電離脂質。通過設計提高DODMA的功效,產生了DLin-MC3-DMA。這是第一個FDA批準的藥物制劑中使用的可電離脂質:siRNA藥物patisiran(Onpattro)。除了有效且安全地遞送siRNA外,DLin-MC3-DMA還用于mRNA的遞送。
目前,學術界和工業界的許多團體使用組合反應方案來合成潛在的傳遞材料,這種方法產生了許多有效的脂質,包括C12-200、503O13、306Oi10、OF-02、TT3、5A2-SC8、SM-102(用于抗SARS-CoV-2的Moderna疫苗mRNA-1273)和ALC-0315(用于輝瑞疫苗BNT162b2)。
除了尋求提高療效外,人們越來越關注提高藥物的特異性,特別是對疫苗和免疫療法的特異性。含有多環金剛烷尾的脂質11-A-M58,和含有環咪唑頭的脂質93-O17S59,已被設計用于體內靶向T細胞。盡管機制尚不清楚,但這些脂質的環狀基團對于靶向T細胞至關重要。
盡管電離脂質可以說是LNP最重要的成分,但其他三種脂質成分(膽固醇、輔助脂質和聚乙二醇化脂質)也促進了納米粒子的形成和功能。膽固醇是一種天然存在的脂質,它通過填充脂質之間的空隙來增強納米顆粒的穩定性,并有助于在攝取到細胞的過程中與內涵體膜融合。
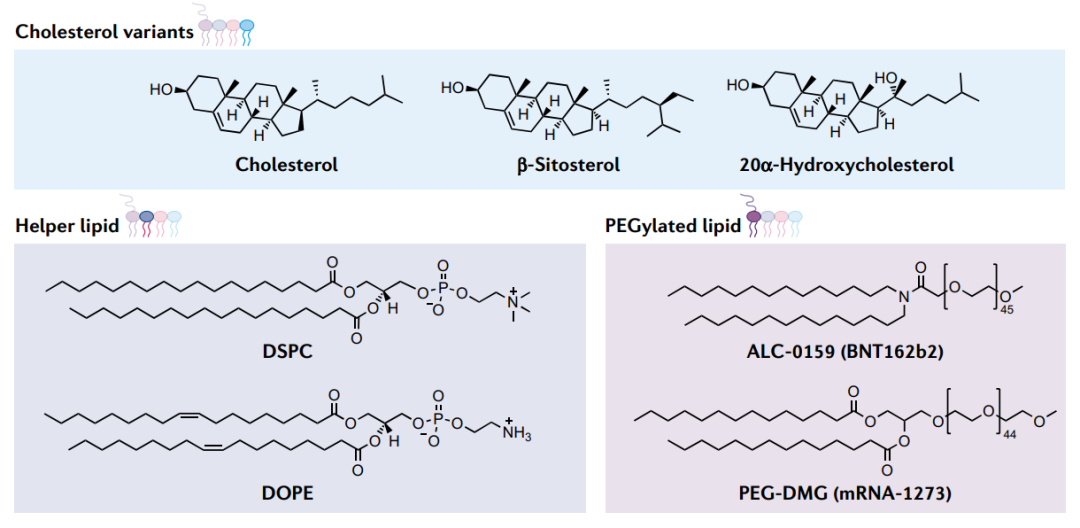
輔助脂質通過促進有助于膜與內涵體融合的脂質相變來調節納米顆粒的流動性并增強功效。最佳輔助脂質的選擇取決于可電離脂質材料和RNA載體。例如,對于類脂質材料,飽和輔助脂質(如DSPC)最適合傳遞短RNA(如siRNA),而不飽和脂質(如DOPE)最適合傳遞mRNA 。DSPC已被用于FDA批準的SARS-CoV-2疫苗mRNA-1273和BNT162b2中。
LNPs的聚乙二醇化脂質成分由聚乙二醇(PEG)與錨定脂質(如DMPE或DMG)結合而成。親水性PEG可以穩定LNP,通過限制脂質融合調節納米顆粒大小,并通過減少與巨噬細胞的非特異性相互作用增加納米顆粒半衰期。mRNA-1273和BNT162b2 SARS-CoV-2疫苗均含有聚乙二醇化脂質。
盡管臨床進展不如LNP,但聚合物具有與脂質相似的優勢,能夠有效傳遞mRNA。基于聚合物的遞送系統由三種聚合物組成,包括陽離子聚合物、樹枝狀聚合物和多糖聚合物。陽離子聚合物將核酸濃縮成具有不同形狀和大小的復合物,可通過內吞作用進入細胞。
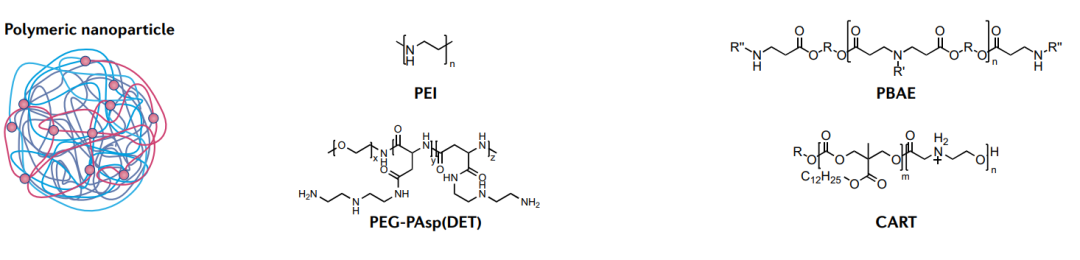
聚乙烯亞胺是研究最廣泛的核酸傳遞聚合物。盡管其功效卓越,但由于其高電荷密度,其毒性限制了應用。此外,已經開發出幾種毒性較小的可生物降解聚合物。例如,聚(β-氨基酯)在mRNA傳遞方面表現出色,尤其是對肺。
最近開發出了一種新型的含脂聚合物,稱為電荷改變可釋放轉運體(CARTs),它能有效地靶向T細胞,操縱T細胞是非常困難的,因此,CART 是一種極具吸引力的傳遞材料,在mRNA疫苗和基因治療領域具有巨大潛力。
脂質體多聚復合物(LPP)納米遞送平臺是一種雙層結構,以聚合物包裹的mRNA分子為核心,包裹在磷脂的雙層外殼中。作為一種非病毒基因遞送載體,LPP結合了聚合物和脂質體的優點,表現出優異的穩定性、降低的細胞毒性、高基因轉染效率以及隨著聚合物降解而逐漸釋放mRNA分子的能力。
病毒樣納米顆粒(VLP)遞送系統是病毒載體和非病毒載體之間的中間體。這些顆粒含有病毒載體的大部分成分,如包膜和衣殼,但沒有病毒基因組。通過病毒工程技術,可以使mRNA結構和病毒衣殼結構蛋白之間特異性識別,從而形成VLP‐mRNA。VLP‐mRNA可以在病毒衣殼和mRNA自身瞬時表達的幫助下有效感染細胞。研究表明,與長時間表達Cas9的病毒系統相比,由VLP‐mRNA遞送的Cas9 mRNA只能存在72小時。因此,脫靶效應的影響可以顯著減少。
Cas9 mRNA的VLP遞送已成功開發出靶向VEGFa,并在年齡相關性黃斑變性小鼠模型中將新生血管面積減少63%。測序結果表明,VLP‐mRNA不會誘導脫靶效應。這些實驗結果有力地支持了VLP在提供CRISPR基因治療方面的臨床應用潛力。
細胞膜包被載體可以模擬細胞膜的性質,將天然細胞膜的特性與納米材料的特性相結合,從而顯著提高生物相容性,同時實現體內長循環和靶向遞送。利用免疫細胞膜,如白細胞、巨噬細胞、中性粒細胞等,已經開發出一系列納米藥物載體。此外,腫瘤細胞和細菌也可以用來制備細胞膜偽裝的納米載體。考慮到腫瘤細胞和細菌表面的特異性蛋白可以激活免疫系統并提高粘附力,這些新型藥物載體在mRNA藥物的功能遞送方面比傳統的納米載體更加多樣化。另外,利用細胞膜上的特異性識別蛋白可以實現靶向藥物遞送到病變部位,為顯著提高治療效果提供了一種新的策略。
作為遞送載體的無機納米材料具有獨特的物理化學性質,如優異的儲存穩定性、良好的生物相容性和易于制備,使其成為mRNA遞送的理想平臺。目前,無機納米結構,包括量子點、二氧化硅納米顆粒(SNPs)、金納米顆粒(AuNP)以及碳基和磁性氧化鐵納米結構,是納米醫學領域最受歡迎的類型。
AuNPs在遞送核酸藥物方面表現出獨特的特性。通過共價或非共價結合,功能部分,如核酸藥物和靶向配體,可以通過硫醇部分共價連接到金納米顆粒核心。AuNPs由于其可調節的尺寸、簡單的功能化、無毒性和免疫惰性,有望成為mRNA遞送的有吸引力的支架。研究顯示,編碼促凋亡因子Bcl-2相關X蛋白的mRNA被AuNPs包裹,顯示出高效的mRNA遞送和抑制異種移植物腫瘤的效力。
然而,無機納米材料在生物體內的長期非特異性積累可能會導致毒性,從而阻礙其大規模臨床應用,因此需要進行詳細的毒理學評估。此外,開發可生物降解和可清除的無機納米材料至關重要。
外泌體是由多泡內小體(MVBs)成熟過程中形成的管腔內小泡(ILV)。當MVB與質膜融合時,ILV被釋放到周質空間,稱為外泌體。外泌體含有大量的特異性蛋白質、脂質、DNA、mRNA、非編碼微小RNA和酶,這是一種新的細胞間通訊模式。因此,外泌體可以作為信使mRNA遞送系統發揮作用。
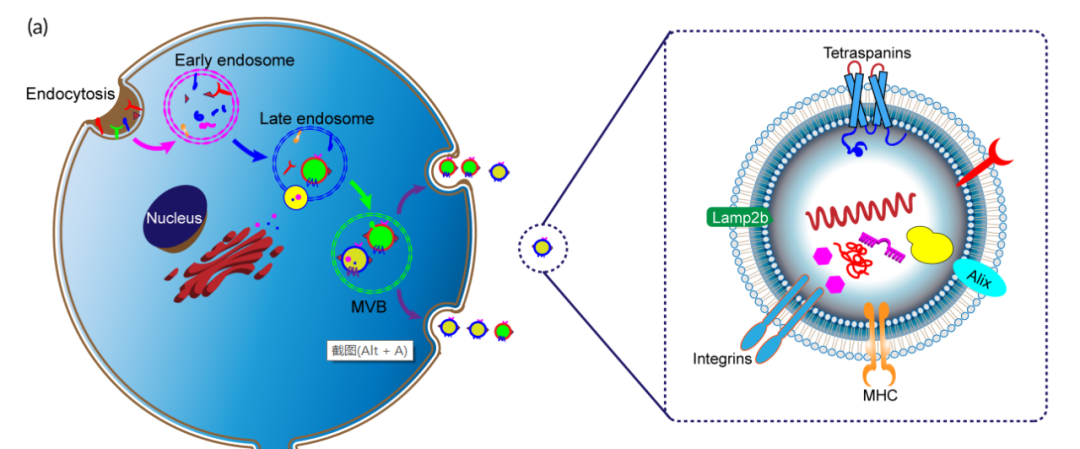
與合成的納米顆粒相比,天然外泌體具有優異的生物相容性和低免疫原性等優異特性。此外,由于外泌體的體積較小,它可以抑制單核吞噬細胞的清除,并在實體瘤部位具有高滲透性和滯留作用,可以在靶點實現藥物積累。外泌體本身可以通過血腦屏障,將藥物輸送到大腦中。特別是鼻內給藥可以促進藥物快速到達腦部病變,為腦部疾病的無創治療提供了可能。
外泌體作為mRNA疫苗的載體越來越受到關注,特別是針對腫瘤的mRNA疫苗,其表面含有MHC的DC衍生細胞外囊泡可增強患者的T細胞免疫應答。此外,與LNPs相比,無論在體內外,外泌體在任何劑量下均無副作用。外泌體將功能性mRNA輸送至人類細胞,也顯示出比LNPs更好的性能。
除了作為mRNA藥物載體外,外泌體的表面功能化還可以實現靶向給藥。修飾的外泌體可以精確地將mRNA分子遞送到靶細胞或器官。總的來說,外泌體具有高度的生物相容性,具有巨大的臨床應用潛力,為mRNA藥物傳遞開辟了新的途徑。
參考文獻:
1. Nanomaterials formRNA‐based therapeutics: Challenges and opportunities. Bioeng Transl Med. 2023 May; 8(3): e10492.
2. mRNA vaccines for infectious diseases: principles, delivery and clinical translation. Nat RevDrug Discov. 2021 Aug 25 : 1–22.
3. Recent advances in mRNA vaccine technology. Curr Opin Immunol. 2020 Aug;65:14-20.






