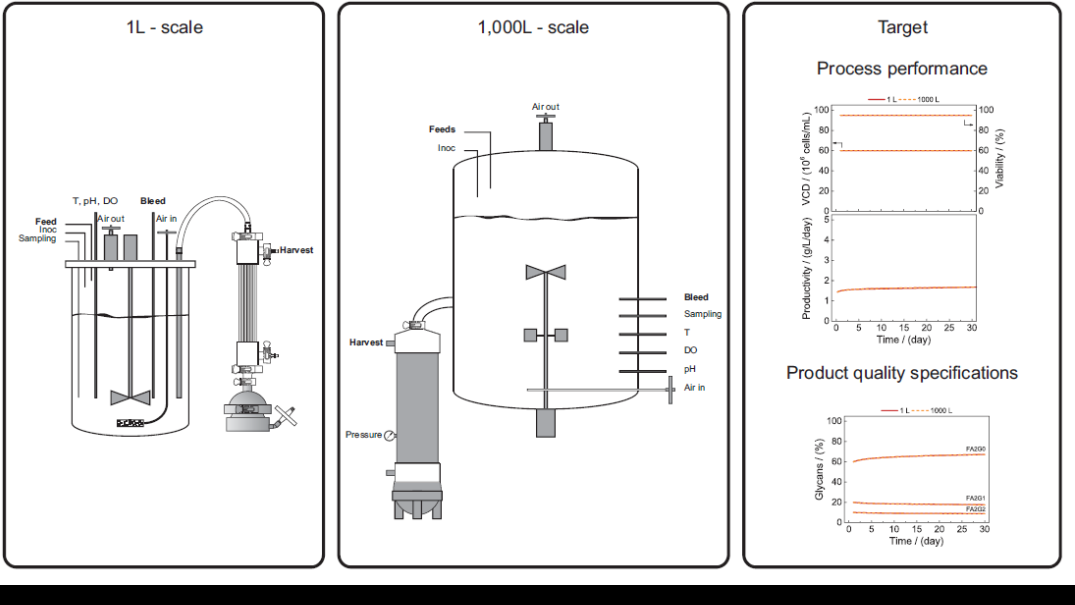
本文將討論灌流生物反應器從幾升的實驗室規模放大到數千升的臨床和商業規模的挑戰。我們考慮實驗室和大型反應器系統之間的比較研究,包括多相反應器模型和計算流體動力學工具以及組學研究,以支持可靠且穩健的放大過程。此外,將討論具體的規模放大問題 - 例如細胞截留裝置長期操作的可放大性以及工藝失敗情況下的批次定義。最后,我們將評估一次性技術的潛力,并以生物生產未來發展背景下的經濟、財務和環境考慮作為本文的結尾
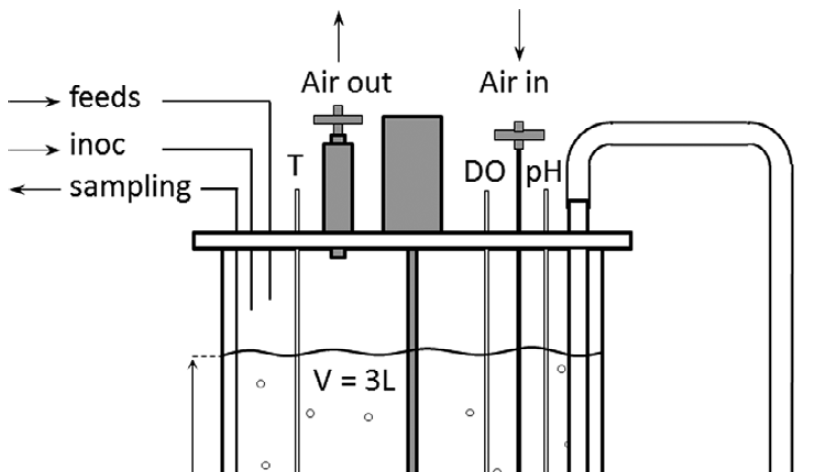
連續灌流培養通常使用與內部或外部細胞分離裝置耦合的攪拌罐生物反應器。前文已經討論了細胞分離裝置的可放大性,這里將重點關注攪拌罐的放大。哺乳動物細胞培養需要特定的工藝設計和設備布局,因為它們具有獨特的特性,主要與對剪切、(非生理)CO2濃度和環境條件變化的高敏感性有關。在下文中,我們將討論關鍵的放大條件 - 即適當的混合、充分的氧氣傳輸以及在低剪切率下充分去除CO2。我們將介紹把工藝設備的特性與工藝
藥物配伍禁忌藥物的配伍禁忌分類:①藥理性(療效性)配伍禁忌指藥理作用相抵觸,如喹諾酮類與氟苯尼考同用藥效降低;②化學性配伍禁忌指引起化學變化,如乙酰水楊酸與堿性藥物配伍引起分解;VC與苯巴比妥配伍引起后者析出;③物理性配伍禁忌如水溶劑與油溶劑配合時分層;含結晶水的藥物配伍時,結晶水析出使固體藥物變成半固體或泥糊狀態。聯合用藥目的①產生協同作用,提高抗菌效果,增強對重癥感染或耐藥性致病菌的療效:②擴
嵌合抗原受體(CAR)T細胞已經復發性血液系統惡性腫瘤的治療中取得了顯著的成功,如急性淋巴細胞白血病(ALL)、非霍奇金淋巴瘤(NHL)和多發性骨髓瘤(MM)。CD19和B細胞成熟抗原(BCMA)是兩種最成功的CAR靶點,具有良好的應答率。靶向CD19的已批準的CAR-T藥物總有效率(ORR)達到70%以上,而靶向BCMA的idecabtagene vicleucel

過繼性T細胞轉移(ACT)是腫瘤治療中最有前途的免疫治療方法之一。目前有四種成熟的ACT技術,包括自體腫瘤浸潤淋巴細胞(TIL)治療、抗原特異性內源性T細胞治療(ETC)、T細胞受體工程T細胞治療(TCR-T)和嵌合抗原受體T細胞治療(CAR-T)。TIL和ETC療法分別依賴于從腫瘤或外周血中分離和體外擴增T細胞,而TCR-T和CAR-T療法利用T淋巴細胞的基因
中性粒細胞是人類中最豐富的免疫細胞,是機體抵御外界微生物的第一道防線。此外,它們也有助于各種生理功能,包括血管生成、凝血和組織修復。最近的研究發現中性粒細胞,特別是中性粒細胞激活后釋放的細胞外陷阱,在系統性自身免疫疾病的發生和持續過程中起著中心作用。然而,由于一些技術挑戰,對中性粒細胞的研究尤其困難。再加上中性粒細胞的半衰期很短(通常不到一天),這些技術問題使中性粒細胞

您可以在此處留言您想要和我們說的話,我們會仔細查看的哦。
在此輸入您的留言內容
